Quand le cholestérol parle au cancer
Longtemps associé aux maladies cardiovasculaires, le cholestérol apparaît aujourd’hui sous un nouveau jour : celui d’un acteur clé dans le développement du cancer. En effet, ses dérivés, appelés oxystérols, jouent un rôle déterminant dans le fonctionnement des cellules. Selon leur nature, ces molécules peuvent soit protéger l’organisme en favorisant la différenciation cellulaire et l’immunité, soit au contraire encourager la croissance tumorale et l’évasion du système immunitaire.
Dans ce contexte, le cancer exploite ces mécanismes à son avantage, détournant certaines voies métaboliques pour assurer sa survie et sa progression. Ce détournement met en évidence l’existence d’un équilibre fragile entre oxystérols protecteurs et délétères, dont la rupture favorise la maladie.
Mieux comprendre cette balance biologique ouvre aujourd’hui de nouvelles perspectives thérapeutiques. Plutôt que de cibler uniquement la tumeur, les chercheurs envisagent désormais de restaurer cet équilibre métabolique afin de réorienter les signaux cellulaires et renforcer les défenses naturelles de l’organisme contre le cancer.
Comprendre le rôle des oxystérols dans notre corps
Le cholestérol est souvent associé à la santé cardiovasculaire. Pourtant, il joue aussi un rôle essentiel dans notre organisme : il constitue les membranes de nos cellules et sert de matière première pour certaines hormones. Mais ce que l’on sait moins, c’est que ses dérivés appelés oxystérols sont de véritables messagers biologiques, capables d’influencer des processus aussi importants que l’immunité… ou le cancer.
Les oxystérols : de petits changements, de grands effets
Les oxystérols sont des molécules dérivées du cholestérol, obtenues par de légères modifications chimiques, notamment l’ajout d’atomes d’oxygène. Bien que ces transformations paraissent minimes, elles entraînent des conséquences majeures sur leur fonction biologique.
En effet, certains oxystérols jouent un rôle bénéfique pour l’organisme. Ils participent à la différenciation des cellules, c’est-à-dire qu’ils aident les cellules à adopter un comportement normal et spécialisé. Par ailleurs, ils renforcent les défenses immunitaires, contribuant ainsi à la protection de l’organisme contre les agressions extérieures, y compris les cellules anormales.
À l’inverse, d’autres oxystérols exercent des effets délétères. Ils peuvent favoriser la croissance des tumeurs en stimulant la prolifération des cellules cancéreuses. De plus, ils participent à des mécanismes qui permettent au cancer d’échapper au système immunitaire, rendant ainsi la maladie plus difficile à combattre.
Ainsi, malgré leur origine commune, les oxystérols peuvent avoir des effets totalement opposés, illustrant à quel point de petites modifications chimiques peuvent profondément influencer le fonctionnement des cellules.
Une balance biologique : bon vs mauvais oxystérols
Un élément central est l’existence, au sein des cellules, d’une véritable « balance » métabolique entre différents types d’oxystérols. Cette balance détermine en grande partie si les cellules vont adopter un comportement normal ou, au contraire, évoluer vers un état pathologique comme le cancer.
Tout commence à partir du cholestérol, qui peut être transformé en intermédiaires appelés 5,6-époxycholestérols. À partir de ces molécules, deux voies métaboliques opposées peuvent être empruntées.
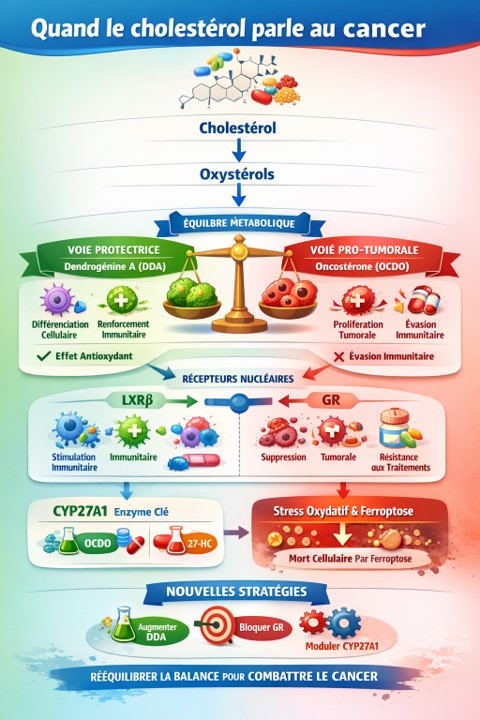
Cholestérol
↓
5,6-époxycholestérols
↓
┌───────────────┬───────────────┐
↓ ↓
Dendrogénine A (DDA) Oncostérone (OCDO)
(protecteur) (favorise cancer)
✔ Différenciation ✖ Prolifération
✔ Immunité ✖ Immunosuppression
✔ Antioxydant ✖ Résistance aux traitements
D’un côté, la production de dendrogénine A (DDA) correspond à une voie protectrice. Cette molécule favorise la différenciation des cellules, stimule le système immunitaire et renforce les mécanismes antioxydants, contribuant ainsi à maintenir un état cellulaire sain.
De l’autre côté, la formation d’oncostérone (OCDO) correspond à une voie délétère. Cette molécule encourage la prolifération des cellules cancéreuses, affaiblit les réponses immunitaires et peut même rendre les cellules plus résistantes aux traitements.
Dans un organisme en bonne santé, ces deux voies sont équilibrées, ce qui permet de réguler correctement le fonctionnement cellulaire. En revanche, dans le contexte du cancer, cet équilibre est rompu : la balance penche en faveur des oxystérols pro-tumoraux, favorisant ainsi la progression de la maladie.
Comment ces molécules influencent les cellules ?
Les oxystérols bioactifs exercent leurs effets en activant des sortes d’« interrupteurs » présents dans les cellules, appelés récepteurs nucléaires. Ces récepteurs contrôlent l’expression de nombreux gènes et orientent le comportement des cellules. Selon le type d’oxystérol impliqué, les conséquences peuvent être bénéfiques ou, au contraire, favoriser le développement du cancer.
D’un côté, certains oxystérols comme la dendrogénine A (DDA) activent un récepteur spécifique nommé LXRβ. Cette activation entraîne plusieurs effets positifs : elle favorise la maturation et la différenciation des cellules, renforce les défenses antioxydantes et stimule l’immunité anti-tumorale. En conséquence, les cellules cancéreuses deviennent plus facilement détectables par le système immunitaire, ce qui facilite leur élimination.
À l’inverse, d’autres oxystérols comme l’oncostérone (OCDO) activent un autre récepteur, le récepteur des glucocorticoïdes (GR). Cette activation soutient la survie des cellules cancéreuses et affaiblit les défenses immunitaires en inhibant notamment les lymphocytes et les cellules NK, essentielles à la destruction des cellules tumorales. Dans ce cas, la tumeur peut se développer plus facilement et échapper aux mécanismes naturels de défense de l’organisme.
Ainsi, en agissant sur ces récepteurs, les oxystérols orientent le destin des cellules, soit vers un état protecteur, soit vers une progression tumorale.
Le rôle du système immunitaire : un champ de bataille
Le système immunitaire joue un rôle central dans la lutte contre le cancer, mais il évolue dans un environnement complexe autour de la tumeur, appelé microenvironnement tumoral. Les oxystérols participent activement à la modulation de cet environnement, influençant directement l’efficacité des défenses immunitaires.
Certains oxystérols, comme la dendrogénine A (DDA), ont un effet stimulant sur le système immunitaire. Ils activent notamment les cellules dendritiques, qui jouent un rôle clé dans l’alerte immunitaire. Ces cellules vont ensuite activer les lymphocytes, capables de reconnaître et de détruire les cellules cancéreuses.
DDA → active l’immunité
↓
Cellules dendritiques → lymphocytes → destruction de la tumeur
À l’inverse, d’autres oxystérols, comme l’oncostérone (OCDO) ou le 27-hydroxycholestérol (27-HC), exercent un effet immunosuppresseur. Ils inhibent l’activité des cellules immunitaires, réduisant ainsi la capacité de l’organisme à combattre la tumeur. Cette diminution des défenses favorise alors la progression du cancer.
OCDO / 27-HC → inhibent l’immunité
↓
Moins de défense → progression du cancer
Ainsi, selon leur nature, les oxystérols peuvent soit rendre la tumeur plus visible et vulnérable aux attaques du système immunitaire, soit au contraire la dissimuler, permettant au cancer de se développer plus facilement.
Une enzyme clé : CYP27A1
Une enzyme joue un rôle particulièrement important dans la régulation de cet équilibre : CYP27A1. Présente dans les cellules, elle intervient dans la transformation des oxystérols et agit comme un véritable « modulateur » de leurs effets biologiques.
Cette enzyme possède une particularité remarquable : elle peut produire des molécules aux effets opposés. D’une part, elle est capable de générer le 27-hydroxycholestérol (27-HC), un oxystérol associé à la progression tumorale dans certains contextes. D’autre part, elle peut aussi transformer des molécules plus dangereuses, comme l’oncostérone (OCDO), en un dérivé anticancéreux, limitant ainsi leurs effets pro-cancéreux.
Ainsi, le rôle de CYP27A1 apparaît comme profondément ambivalent. Selon le contexte biologique et l’équilibre des autres voies métaboliques, elle peut soit contribuer au développement du cancer, soit au contraire participer à des mécanismes de protection.
Oxydation et stress : un lien avec la mort cellulaire
Les oxystérols sont étroitement liés au stress oxydatif, un déséquilibre chimique qui survient lorsque les cellules produisent trop de molécules réactives (appelées radicaux libres) et ne parviennent plus à les neutraliser efficacement. Ce phénomène est fréquent dans de nombreuses maladies, notamment le cancer, et modifie profondément le fonctionnement cellulaire.
Dans ce contexte, les oxystérols pourraient jouer un rôle dans un type particulier de mort cellulaire appelé ferroptose, un mécanisme dépendant du fer et caractérisé par l’oxydation des lipides des membranes. Ce processus attire aujourd’hui beaucoup l’attention des chercheurs, car il représente une voie potentielle pour éliminer les cellules cancéreuses.
Cependant, à l’heure actuelle, les données scientifiques restent encore incomplètes. Les travaux suggèrent fortement l’existence d’un lien entre oxystérols, stress oxydatif et ferroptose, mais ce lien n’est pas encore totalement démontré. Des recherches supplémentaires seront nécessaires pour comprendre précisément comment ces mécanismes interagissent et dans quelles conditions ils pourraient être exploités à des fins thérapeutiques.
Pourquoi c’est important pour la médecine ?
Ces avancées scientifiques ont des implications majeures pour la médecine, en particulier dans le domaine de la lutte contre le cancer. Elles ouvrent la voie à de nouvelles stratégies thérapeutiques qui ne se limitent plus à détruire directement les cellules tumorales, mais cherchent à rééquilibrer les mécanismes internes qui contrôlent leur comportement.
Une première approche consiste à restaurer l’équilibre entre les différents oxystérols. Il s’agirait d’augmenter la production de molécules protectrices, comme la dendrogénine A (DDA), tout en réduisant la formation de molécules pro-tumorales, telles que l’oncostérone (OCDO). En rétablissant cette balance, on pourrait freiner la progression du cancer et favoriser des réponses cellulaires plus normales.
Une seconde stratégie repose sur le ciblage des récepteurs activés par ces oxystérols. Par exemple, stimuler le récepteur LXRβ pourrait renforcer les effets anticancéreux en favorisant la différenciation cellulaire et l’immunité. À l’inverse, bloquer le récepteur des glucocorticoïdes (GR), impliqué dans les effets pro-tumoraux, pourrait limiter la survie et la résistance des cellules cancéreuses.
Enfin, une troisième piste consiste à agir directement sur le métabolisme des lipides, en ciblant les enzymes impliquées dans la transformation des oxystérols, comme CYP27A1. En modulant l’activité de ces enzymes, il serait possible d’influencer la production des différentes molécules et, ainsi, de réorienter les signaux cellulaires dans un sens favorable à la lutte contre le cancer.
Ces différentes approches illustrent une nouvelle manière de penser les traitements : non plus seulement attaquer la tumeur, mais rééquilibrer les processus biologiques qui la favorisent.
En conclusion, les oxystérols mettent en lumière une idée particulièrement intéressante : le cancer ne peut pas être considéré uniquement comme une maladie d’origine génétique. Il possède également une dimension métabolique, liée aux transformations chimiques qui se produisent au sein des cellules.
Pour en savoir plus
Semin Cancer Biol . 2026 Mar 14:121:22-32.doi: 10.1016/j.semcancer.2026.03.001. Online ahead of print.
Oxysterols at the crossroads of cholesterol metabolism and cancer
Julio Buñay, Silia Ayadi, Chloe Gressein, Philippe de Medina, Sandrine Silvente-Poirot, Marc Poirot
Equipe INOV Métabolisme du cholestérol et innovations thérapeutiques.



