Reprogrammer une famille de lipides pour augmenter l’efficacité de l’immunothérapie du mélanome.
ceramide
metabolisme
Anti PD-1
anti-CTLA-4
immunothérapie du mélanome
résistance des mélanomes
Bruno Ségui & Céline Colacios Equipe du CRCT : Ceramide metabolism in melanoma
L’immunothérapie du mélanome avancé a révolutionné la prise en charge thérapeutique de ce cancer redoutable. Toutefois, près de la moitié des patients ne répond pas à ce traitement et décède dans les 5 ans suivant le début du traitement. Nos travaux montrent que les cellules de mélanome présentent des altérations du métabolisme d’une famille de lipides, les sphingolipides, qui contribuent à la résistance aux immunothérapies. Nous proposons une stratégie originale pour reprogrammer ce métabolisme en exprimant dans les cellules de mélanome une enzyme, la sphingomyélinase neutre 2, qui stimule la réponse immunitaire contre les cellules cancéreuses et les sensibilise aux immunothérapies dans des modèles précliniques de mélanome. Chez les patients atteints de mélanome avancé, l’expression de cette enzyme dans les biopsies tumorales est associée à un bon pronostic.
Ce travail contribue au rationnel scientifique d’IMMUSPHINX (NCT03627026), un essai clinique réalisé chez 60 patients atteints de mélanome avancé traités par immunothérapie (nivolumab associé, ou non, à l’ipilimumab ; pembrolizumab) . L’objectif primaire d’IMMUSPHINX est de prédire la réponse des patients aux immunothérapies en établissant des signatures du métabolisme des sphingolipides à partir de biopsies tumorales et de prélèvements sanguins. Cet essai, promu par l’Institut Claudius Regaud, a débuté en Janvier 2019 et est financé dans le cadre d’un projet Européen (ERA-NET Transcan-2 H2020).
Ce travail fait l’objet d’un brevet : WO2017134116A1 : Procédés et compositions pharmaceutique pour amplifier des réponses immunitaires dépendantes des lymphocytes T CD8+ chez des sujets souffrant de cancer.
Collaborations et remerciements
INSERM, Université Toulouse III- Paul Sabatier, Ligue Nationale Contre le Cancer (LNCC, Equipe Labellisée 2013), Ligue Régionale Contre le Cancer (Midi-Pyrénées), INSERM Transfert, Cancéropôle Grand Sud-Ouest, ROTARY Toulouse clubs, Fondation Toulouse Cancer Santé, Fondation ARC (Equipe Labellisée 2019), Transcan-2 Research Program (ERA-NET Transcan-2), Marie Curie Actions, Fondation de France, laboratoire d’excellence Toulouse Cancer (LABEX TOUCAN)
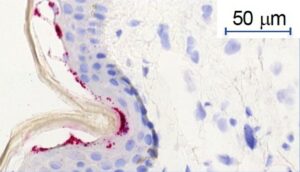
Une image
Découvrir l’article publié
Cancer Immunol Res. 2021 Mar 16:canimm.0342.2020. doi: 10.1158/2326-6066.CIR-20-0342. Online ahead of print.
Neutral sphingomyelinase 2 heightens anti-melanoma immune responses and anti-PD-1 therapy efficacy.
Montfort A, Bertrand F, Rochotte J, Gilhodes J, Filleron T, Milhès J, Dufau C, Imbert C, Riond J, Tosolini M, Clarke CJ, Dufour F, Constantinescu AA, de França Junior N, Garcia V, Record M, Cordelier P, Brousset P, Rochaix P, Silvente-Poirot S, Therville N, Andrieu-Abadie N, Levade T, Hannun YA, Benoist H, Meyer N, Micheau O, Colacios C, Ségui B.

Centre de Recherches en Cancérologie de Toulouse (Oncopole)
Toulouse – FR
Nous contacter
05 82 74 15 75
Envie de rejoindre
L’équipe du CRCT ?